74431 skanuj0004 (254)

445
14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej
i
i

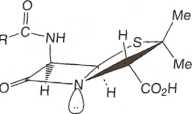
ki sugeruje, źe pochodzi ona od aminokwasów cysteiny i waliny (iys. 14.19), i to też ustalono. Kształt cząsteczki przypomina wpół otwartą książkę (rys. 14.20).
Acylowy łańcuch boczny (R) może być różny i zależy od środowiska fermentacji. Kiedy na przykład w Stanach Zjednoczonych rozpoczęto produkcję penicyliny na dużą skalę, zastosowano namoczoną kukurydzę; otrzymano wówczas penicylinę G (R =* benzyl), co było możliwe dzięki wysokiemu poziomowi kwasu fenylooctowego w środowisku.
Analogi penicyliny
Jedna z metod różnicowania łańcucha bocznego polega na dodaniu różnych kwasów karboksylowych do środowiska fermentacyjnego; na przykład dodanie kwasu fenoksyoctowego (Ph0CH2C02H) daje penicylinę V (rys. 14.18).
Rodzaj kwasów karboksylowych, które można dodać do środowiska, jest jednak ograniczony (np. tylko kwasy o wzorze ogólnym RCH2CO2H), i to z kolei ogranicza rodzaj możliwych do uzyskania analogów. Inną dość dużą niedogodnością tej metody jest jej monotonność i czasochłonność.
W 1957 roku Sheehan otrzymał penicylinę syntetyczną. W wyniku wieloetapowej syntezy z 1-proc. wydajnością uzyskał penicylinę V. Niestety, pełna synteza nie była skutecznym sposobem na otrzymywanie analogów penicyliny.
W latach 1958-1960 Beechams opanował izolowanie biosyntetycznej substancji pośredniej penicyliny, która była także jednym z produktów pośrednich w syntezie Sheehana. Związkiem tym był 6-APA; dzięki niemu można było zastosować metodę półsyntetyczną do syntezy olbrzymiej liczby analogów. Tak więc w wyniku fermentacji uzyskano 6-APA, który następnie wykorzystano w syntezie analogów penicyliny, acylując 6-APA różnymi chlorkami kwasowymi (rys. 14.21).
Obecnie 6-APA uzyskuje się (rys. 14.22) w procesie enzymatycznej hydrolizy penicyliny G lub penicyliny V (acylaza penicylinowa) lub metodami chemicznymi (patrz dalej). Metody te są wydajniejsze niż proces fermentacji.
Skoncentrowaliśmy się na analogach penicyliny ze zróżnicowanymi acylo-wymi łańcuchami bocznymi. Bez wahania można zadać pytanie: dlaczego? Czy penicylina nie jest wystarczająco dobra? Poza tym, co jest szczególnego w acy-lowym łańcuchu bocznym? Czy nie można dokonać zmian także w innych miejscach cząsteczki?
Wyszukiwarka
Podobne podstrony:
skanuj0020 (74) 461 14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej ryny mogą s
skanuj0024 (57) 465 14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej •
skanuj0028 (48) 469 14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej Lek ten jes
skanuj0016 (96) 457 14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej grupę amino
skanuj0002 (269) 443 14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej W 1928 rok
27165 skanuj0010 (165) 451 14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej Wraż
skanuj0008 (186) 14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej 449 atomie
29569 skanuj0022 (64) 14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej 463 kznyc
85780 skanuj0030 (41) 14.5. Związki przedwbakteryjne zaburzające syntezę ściany komórkowej Otrzymano
więcej podobnych podstron